蛋白質濃度測定的方法有很多,考馬斯亮藍測定蛋白質是其中一種方式,它利用比色法檢測,操作簡便。

實驗原理 :
考馬斯亮藍 (Coomassie Brilliant Blue) 法測定蛋白質濃度,是利用蛋白質—染料結合的原理,可定量測定微量蛋白濃度快速、靈敏的方法。
考馬斯亮藍 R-250 染料,在酸性溶液中與蛋白質結合,使染料的最大吸收峰 (lmax) 的位置,由 465 nm 變為 595 nm,溶液的顏色也由綠黑/藍黑色變為藍色。 通過測定 595 nm 處光吸收的增加量可知與其結合蛋白質的量。 研究發現,染料主要是與蛋白質中的鹼性氨基酸 (特別是精氨酸) 和芳香族氨基酸殘基相結合。

碗盤洗乾淨後色素較不會附著。
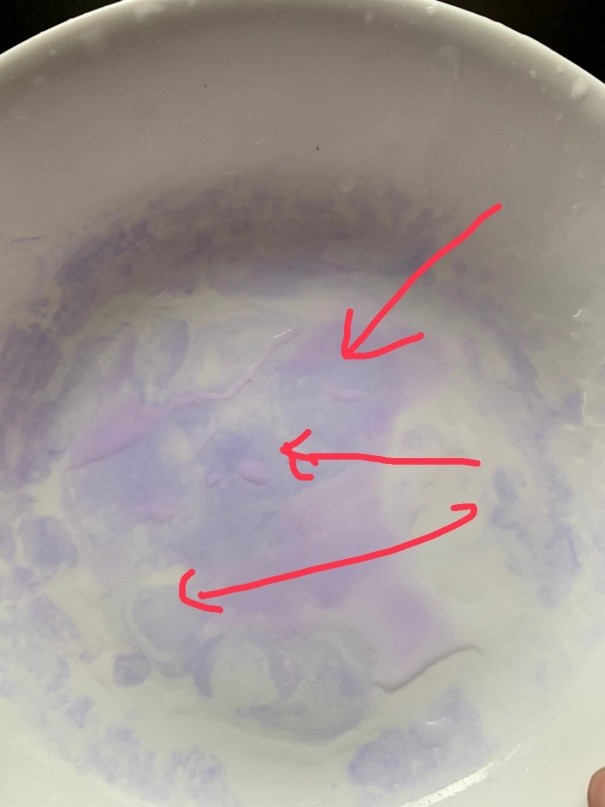
顯著藍色表示有蛋白質殘留。
此法的突出優點
(1)快速、簡便、靈敏度高,據估計比 Lowry 法約高四倍,其最低蛋白質檢測量可達 1 mg。 這是因為蛋白質與染料結合後產生的顏色變化很大,蛋白質-染料複合物有更高的消光係數,因而光吸收值隨蛋白質濃度的變化比 Lowry 法要大的多。
(2)操作容易,只需加一種試劑。 完成一個樣品的測定,只需要 5 分鐘左右。 由於染料與蛋白質結合的過程,大約只要 2 分鐘即可完成,其顏色可以在 1 小時內保持穩定,且在 5 分鐘至 20 分鐘之間,顏色的穩定性最好。 因而完全不用像 Lowry 法那樣費時和需要嚴格地控制時間。
(3)干擾物質少。 如干擾 Lowry 法的 K+、Na+、Mg2+ 離子、Tris 緩衝液、糖和蔗糖、甘油、巰基乙醇、EDTA 等均不干擾此測定法。
此法的缺點
(1)由於各種蛋白質中的精氨酸和芳香族氨基酸的含量不同,因此考馬斯亮藍染色法用於不同蛋白質測定時有較大的偏差,在製作標準曲線時通常選用 g-球蛋白為標準蛋白質,以減少這方面的偏差。
(2)仍有一些物質干擾此法的測定,主要的干擾物質有:去汙劑、 Triton X-100、十二烷基硫酸鈉 (SDS) 等。
測試方法 :
1 試劑
考馬斯亮藍試劑:
考馬斯亮藍 R-250 10 mg 溶於 5 mL 95% 乙醇中,加入 10 mL 85% 磷酸,用蒸餾水稀釋至 100 mL。
2 將考馬斯亮藍試劑均勻噴灑於碗盤,沒有噴灑到的地方,旋轉碗盤使試劑均勻分布於完盤上。
3. 觀察碗盤上的考馬斯亮藍試劑的顏色,若碗盤呈現顯著藍色表示有蛋白質殘留。

碗盤洗乾淨後色素較不會附著。

顯著藍色表示有蛋白質殘留。
注意事項
(1)在試劑加入後的 5-20 min 內判讀,因為在這段時間內顏色是最穩定的。
(2)測定中,蛋白-染料複合物會有少部分吸附於碗盤壁上,測定完後可用乙醇將藍色的殘留洗乾淨。